研究紹介
シトクロムP450を利用するバイオ触媒の開発
第2章: デコイ分子を用いたP450BM3等の機能改変
第12話「マンガンを中心に持つヘム置換P450BM3の反応特性調査」
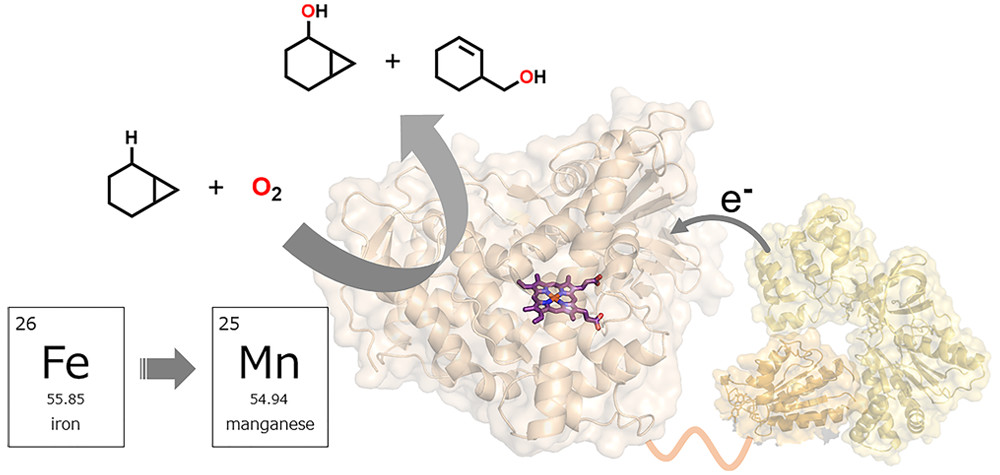
我々は以前に、P450BM3を構成するヘムドメインと還元ドメインを別々に発現し、ヘムドメインのヘム(鉄錯体)を別の中心金属を持つヘム類縁体に置換することで、マンガンを始めとする複数のヘム置換P450BM3の作製に成功した (研究紹介P450BM3第5話)。また、マンガンを中心金属に持つP450BM3では、天然の鉄含有P450BM3と同様に、酸素分子を活性化し、デコイ分子存在下でプロパン等の非天然基質の水酸化が可能であり、これはマンガンを活性中心とする金属酵素では非常に稀な例であった。しかし、その触媒効率は天然の鉄中心のものと比較して低く、また、その反応機構についても未解明であった。
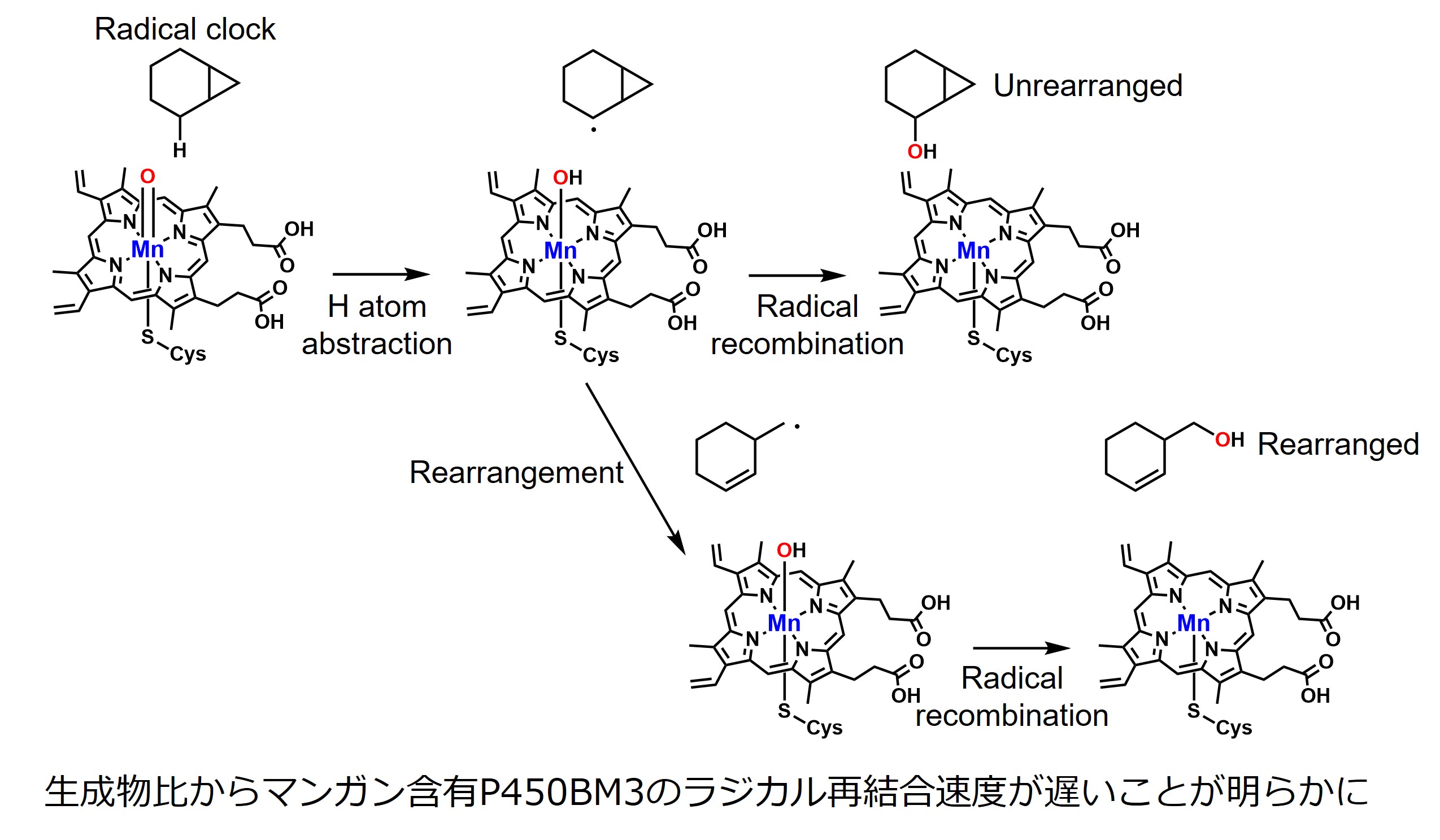
そこで、まず、マンガン含有P450BM3でデコイ分子存在下でシクロヘキサンの水酸化を16O2(一般的な酸素分子)と、18O2で反応を行なったところ、生成物のシクロヘキサノールに18Oが取り込まれたことから酸素分子を酸素源として使用していることを確認した。また、P450BM3のヘムへの軸配位子であるCys400の隣に位置するIle400をProに置換したI401P変異がマンガン含有P450BM3の触媒効率の向上に有用であることを発見した。さらにマンガン含有P450BM3の反応特性の理解のために、既知のラジカルクロック分子(1-methyl-2-phenylcyclopropane, Norcarane)を基質として、水酸化反応を行ったところ、その反応機構は天然の鉄中心P450BM3と同様の水素原子引き抜き/ラジカル再結合であると示された。また、2種類の生成物の比から、酸化活性種のラジカル再結合のスピードを見積もったところ、天然の鉄中心P450BM3に比べて、マンガン含有P450BM3はラジカル再結合が遅いことが明らかとなり、天然の鉄中心P450BM3とは異なる反応特性を有していることを明らかにした。
詳細はこちらの論文をご参照下さい。
- K. Omura, Y. Aiba, K. Suzuki, S. Ariyasu, H. Sugimoto, O. Shoji "A P450 Harboring Manganese Protoporphyrin IX Generates a Manganese Analogue of Compound I by Activating Dioxygen" , ACS Catal., 12, (2022) 11108-11117.
https://doi.org/10.1021/acscatal.2c01345